Una dieta alta en grasas puede tener un impacto directo en el desarrollo del cáncer de mama triple negativo.
Se trata de un tipo de tumor que no presenta receptores de estrógeno, progesterona ni HER2 en sus células, lo que dificulta su tratamiento con terapias hormonales o dirigidas.
Investigadores de la Universidad de Princeton de los Estados Unidos demostraron que el entorno con más lípidos acelera el crecimiento y la invasión tumoral. Los resultados se publicaron en la revista APL Bioengineering.

Usaron un modelo microfluídico tridimensional que simula el flujo real de nutrientes en el cuerpo.
Se cultivaron células de cáncer de mama triple negativo bajo cinco condiciones distintas: basal, alta insulina, alta glucosa, alta cetona y alta grasa.
El objetivo fue observar cómo responde el tumor frente a diferentes estados metabólicos y si la presencia de más lípidos cambia su comportamiento.

“Adoptamos el enfoque de construir tumores idénticos diseñados y cultivarlos en condiciones que imitan la composición de la sangre de pacientes bajo diferentes estados dietéticos”, dijo la autora principal Celeste Nelson.
“Esperábamos identificar condiciones dietéticas que enlentecieran el crecimiento tumoral. En cambio, encontramos una condición dietética, una dieta alta en grasas, aceleró el crecimiento tumoral.”
Cuando la dieta cambia el destino tumoral

Los investigadores buscaron superar las limitaciones de los modelos tradicionales.
En la mayoría de los experimentos previos, los cultivos celulares y los modelos animales no reproducen ni el flujo constante de nutrientes ni la complejidad real del entorno humano.
Para aislar el efecto de los lípidos, se utilizó un medio enriquecido con 4% de albúmina rica en lípidos, simulando una condición hiperlipidémica.

El foco estuvo en analizar si una dieta alta en grasas modifica la estructura, el crecimiento y la invasión de las células tumorales en comparación con otros escenarios bioquímicos representativos de estados posprandiales, diabéticos y cetogénicos.
El modelo permitió ver cómo los cambios bioquímicos influyen en la motilidad celular y en la expresión de genes que favorecen la invasión y la remodelación de la matriz extracelular.
Así se buscó entender si el entorno rico en lípidos vuelve a las células más agresivas.
Cómo se hizo el estudio y qué se halló
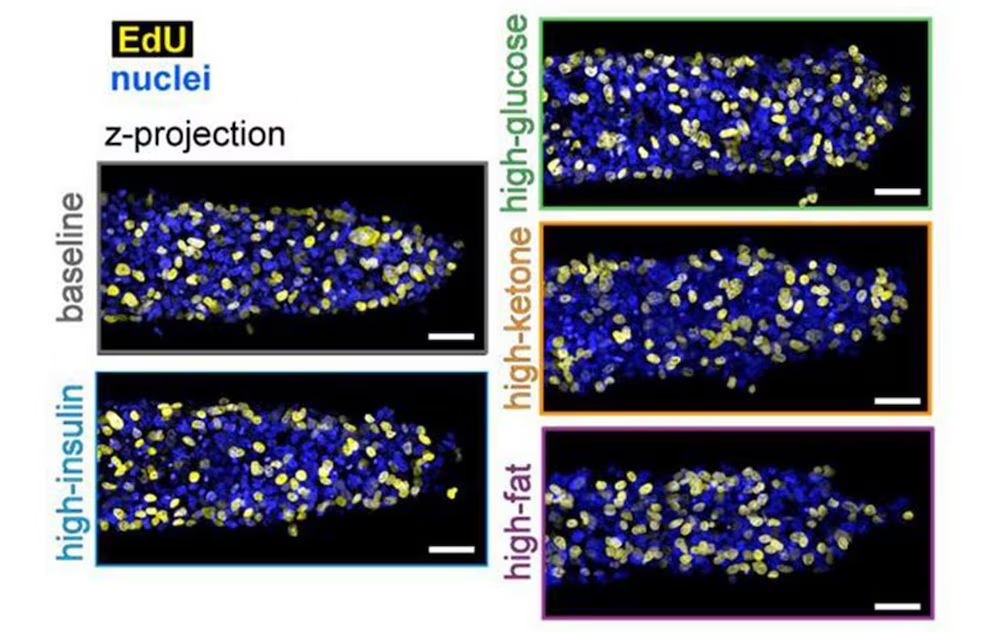
Las células de cáncer de mama triple negativo mostraron tasas de proliferación y morfología similares en las cinco condiciones cuando se cultivaron en dos dimensiones.
Sin embargo, al crecer en el modelo tridimensional, los tumores bajo condiciones altas en grasa se volvieron más grandes e invasivos.
“En el modelo microfluídico 3D, las condiciones altas en grasa aceleran el crecimiento y la invasión tumoral y provocan la formación de cavidades huecas”, señalaron los investigadores.
Estas cavidades se formaron en el interior de los tumores a partir del sexto día de cultivo, mientras que los tumores en condiciones basales se mantuvieron sólidos.
El análisis genético reveló que la expresión del gen MMP1 aumentó en ambientes con alto contenido de lípidos. MMP1 es una enzima que degrada la matriz extracelular y favorece la diseminación celular.
A pesar del mayor tamaño y la invasión, no se detectó un aumento en la proliferación ni en la muerte celular por apoptosis o ferroptosis.
El estudio lo resume: “Nuestros resultados muestran que los tumores con alta grasa forman regiones huecas sin aumentar la proliferación o muerte celular”.
El equipo también midió la fuente de energía celular. Bajo condiciones altas en grasa, las células tumorales dependieron más de la fosforilación oxidativa, un proceso que ocurre en las mitocondrias y produce energía a partir de oxígeno, en comparación con la glucólisis, que predominó en otras condiciones.
El análisis descartó que la viscosidad del medio fuese responsable de los cambios observados, lo que refuerza que la composición química es la causa principal del comportamiento más agresivo.
Limitaciones, recomendaciones y futuro

El modelo desarrollado no incluye la respuesta inmune ni la microbiota, factores presentes en el cuerpo humano que también influyen en el desarrollo tumoral.

Los investigadores reconocen que sus hallazgos representan solo una parte de la compleja relación entre dieta y cáncer.
El equipo planea evaluar si los tumores responden de manera diferente a la quimioterapia bajo distintas condiciones dietéticas.
El uso de modelos que simulan el flujo real de nutrientes permite ver conexiones antes invisibles entre la alimentación y el cáncer de mama triple negativo.
La investigación concluyó que replicar el entorno bioquímico del plasma humano en laboratorio puede ayudar a entender mejor el impacto de la dieta en el destino tumoral y abrir puertas para el diseño de nuevas estrategias clínicas.
Ahora se espera aplicar el enfoque a otros subtipos de cáncer de mama y a diferentes terapias para ampliar las posibilidades en los tratamientos futuros.